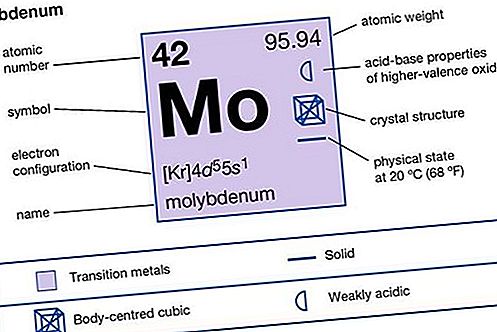
Periooditabeli 6. rühma (VIb) keemiline element, hõbehall hall tulekindel metall - molübdeen (Mo), mida kasutatakse terase ja muude sulamite parema tugevuse saamiseks kõrgel temperatuuril.
Rootsi keemik Carl Wilhelm Scheele näitas (umbes 1778), et mineraal molübdaina (nüüd molübdeniit), mida pikka aega peeti pliimaagiks või grafiidiks, sisaldab kindlasti väävlit ja võib-olla ka varem tundmatut metalli. Scheele'i soovitusel isoleeris teine Rootsi keemik Peter Jacob Hjelm metalli (1782) edukalt ja nimetas selle Kreeka molübdoodidest molübdeeniks "plii".
Molübdeeni ei leidu looduses vabaks. Suhteliselt haruldane element, see on umbes sama rikkalik kui volfram, mida see sarnaneb. Suhe molübdeeni peatoimetaja maaki molybdenite-molübdeendisulfiid, meremagustraalide 2 but molübdaadid nagu pliimolübdaadi, PbMoO 4 (wulfenite) ja MgMoO 4 leidub ka. Enamik kaubanduslikku toodangut saadakse maagidest, mis sisaldavad mineraalset molübdeniiti. Kontsentreeritud mineraal röstitakse tavaliselt õhu ülejäägis, et saada molübdeentrioksiid (MoO 3), mida nimetatakse ka tehniliseks molübdeenoksiidiks, mida pärast puhastamist saab vesinikuga redutseerida metalli moodustamiseks. Edasine ravi sõltub molübdeeni lõplikust kasutamisest. Molübdeeni võib ahjus olevale terasele lisada kas tehnilise oksiidi või ferromolübdeeni kujul. Ferromolübdeeni (sisaldab vähemalt 60 protsenti molübdeeni) saadakse tehnilise oksiidi ja raudoksiidi segu süütamisel. Metallilise molübdeeni toodetakse pulbri vesiniku redutseerimisel keemiliselt puhas molübdeenoksiidiks või Ammooniummolübdaadil, (NH 4) 2 MoO 4. Pulber muundatakse massmetalli metalliks pulbermetallurgia või kaarvaluprotsessi abil.
Molübdeeni aluselised sulamid ja metall ise on kasuliku tugevusega temperatuuridel, millest kõrgem on enamik teisi metalle ja sulameid. Molübdeeni peamine kasutusala on aga legeeriv osa raud- ja värviliste sulamite tootmisel, millele see annab ainulaadse kuumuse tugevuse ja korrosioonikindluse, nt reaktiivmootorites, põlemisvooderdustes ja järelpõletusdetailides. See on raua ja terase kõvaduse suurendamise üks tõhusamaid elemente ning lisaks sellele karastatud ja karastatud terase vastupidavus. Kõrget korrosioonikindlust, mida on vaja ravimite töötlemiseks kasutatavates roostevabades terastes ja autotööstuses kasutatavates kroomiterastes, suurendavad unikaalselt molübdeeni väikesed lisandid. Metallilist molübdeeni on kasutatud selliste elektriliste ja elektrooniliste osade jaoks nagu hõõgniidi toed, anoodid ja võred. Varrast või traati kasutatakse elektriahjude kuumutamisel temperatuuril kuni 1700 ° C (3,092 ° F). Molübdeeni katted kleepuvad kindlalt terase, raua, alumiiniumi ja muude metallidega ning on suurepärase kulumiskindlusega.
Molübdeen on hapete, eriti kontsentreeritud lämmastik- ja vesinikfluoriidhapete segude suhtes üsna vastupidav, ja seda saab kiiresti rünnata aluseliste oksüdeerivate sulate abil, näiteks sulatatud kaaliumnitraadi ja naatriumhüdroksiidi või naatriumperoksiidi segudega; vesialused pole aga mõju. Normaalsel temperatuuril on see hapniku suhtes inertne, kuid kombineerub sellega punase kuumuse juures kergesti, saades trioksiide, ja toatemperatuuril ründab fluori, saades heksafluoriide.
Looduslik molübdeen on segu seitsmest stabiilsest isotoobist: molübdeen-92 (15,84 protsenti), molübdeen-94 (9,04 protsenti), molübdeen-95 (15,72 protsenti), molübdeen-96 (16,53 protsenti), molübdeen-97 (9,46 protsenti), molübdeen-98 (23,78 protsenti) ja molübdeen-100 (9,13 protsenti). Molübdeeni oksüdeerumisseisundid on vahemikus +2 kuni +6 ja karbonüül Mo (CO) 6 oksüdatsiooni olekuks loetakse nulli. Molübdeen (+6) on trioksiidis, mis on tähtsaim ühend, millest valmistatakse suurem osa teistest selle ühenditest, ja molübdeesides (mis sisaldavad aniooni MoO 4 2 -), mida kasutatakse pigmentide ja värvainete tootmiseks. Grafiiti meenutavat molübdeendisulfiidi (MoS 2) kasutatakse tahke määrdeainena või määrdete ja õlide lisandina. Molübdeen moodustab boori, süsiniku, lämmastiku ja räniga kõvasid, tulekindlaid ja keemiliselt inertseid interstitsiaalseid ühendeid nende elementidega otsesel reaktsioonil kõrgel temperatuuril.
Molübdeen on taimedes oluline mikroelement; kaunviljades kui katalüsaatoris aitab see bakteritel lämmastikku kinnistada. Molübdeentrioksiidi naatriummolübdaadi (Na 2 MoO 4) on kasutatud mikrotoitaineid.
Suurimad molübdeeni tootjad on Hiina, USA, Tšiili, Peruu, Mehhiko ja Kanada.
Elemendi omadused
| aatomnumber | 42 |
|---|---|
| aatommass | 95,94 |
| sulamispunkt | 2610 ° C (4730 ° F) |
| keemispunkt | 5560 ° C (10,040 ° F) |
| erikaal | 10,2 temperatuuril 20 ° C (68 ° F) |
| oksüdatsiooniseisundid | 0, +2, +3, +4, +5, +6 |
| elektronide konfiguratsioon | [Kr] 4d 5 5s 1 |