Ravimite avastamine ja arendamine
Ravimite väljatöötamise protsess
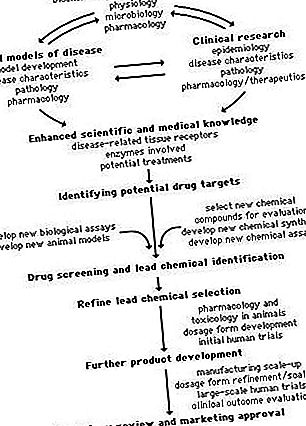
Keemiliste ühendite tuvastamiseks, mida võib välja töötada ja turustada, kasutatakse mitmesuguseid lähenemisviise. Farmaatsiatoodete arendamiseks vajalike keemiliste ja bioloogiliste teaduste praegune olukord nõuab, et 5000–10 000 keemilist ühendit tuleb iga inimesele kasutamiseks heaks kiidetud uue ravimi laboratoorsel skriinimisel läbi viia. Skriinitud 5000–10 000 ühendist läheb prekliinilisse uuringusse umbes 250 ja 5 kliinilisse uuringusse. Kogu protsess alates ravimi avastamisest kuni turustamiseni võib kesta 10–15 aastat. Selles jaotises kirjeldatakse mõnda protsessi, mida tööstuses kasutatakse uute ravimite avastamiseks ja väljatöötamiseks. Voodiagramm sisaldab selle arendusprotsessi üldist kokkuvõtet.
Uurimine ja avastamine
Farmaatsiatooteid toodetakse mitmesuguste ravimite väljatöötamise ja tootmisega tegelevate avaliku ja erasektori organisatsioonide hulga tegevuste tulemusel. Selle protsessi osana viivad paljude riiklikult rahastatavate asutuste teadlased läbi põhiuuringuid sellistes valdkondades nagu keemia, biokeemia, füsioloogia, mikrobioloogia ja farmakoloogia. Alusuuringud on peaaegu alati suunatud looduslike ainete või füsioloogiliste protsesside uue mõistmise arendamisele, mitte aga konkreetse toote või leiutise väljatöötamisele. See võimaldab riigiasutuste ja erasektori teadlastel rakendada uusi teadmisi uute toodete väljatöötamisel. Selle protsessi esimesed sammud viivad läbi põhiteadlased ja arstid, kes töötavad erinevates teadusasutustes ja ülikoolides. Nende uuringute tulemused avaldatakse teadus- ja meditsiiniajakirjades. Need tulemused hõlbustavad uimastite avastamise võimalike uute sihtmärkide tuvastamist. Sihtmärkideks võivad olla ravimiretseptor, ensüüm, bioloogiline transpordiprotsess või mõni muu keha metabolismis osalev protsess. Kui sihtmärk on kindlaks tehtud, teostavad või suunavad ravimiosad suuremat osa ravimi avastamise ja väljatöötamisega seotud tööst.
Teaduslike teadmiste panus ravimite avastamisse
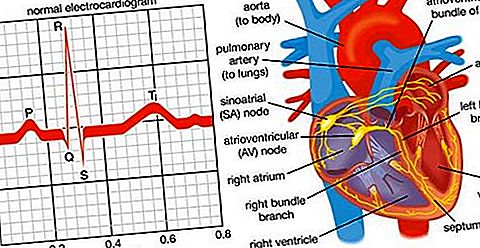
Kaks antihüpertensiivsete ravimite klassi on näide sellest, kuidas ühe kehasüsteemi täiendatud biokeemilised ja füsioloogilised teadmised aitasid kaasa ravimite väljatöötamisele. Hüpertensioon (kõrge vererõhk) on südame-veresoonkonna haiguste peamiseks riskiteguriks. Kardiovaskulaarsete haiguste ennetamise oluline viis on kõrge vererõhu kontrollimine. Üks vererõhu kontrolliga seotud füsioloogilistest süsteemidest on reniin-angiotensiinisüsteem. Reniin on neerudes toodetav ensüüm. See toimib angiotensiini tootmiseks verevalgule. Selle süsteemi biokeemia ja füsioloogia üksikasjad töötasid välja biomeditsiini teadlased, kes töötavad haiglates, ülikoolides ja valitsuse uurimislaborites kogu maailmas. Kaks olulist etappi reniini-angiotensiinisüsteemi füsioloogilise toime saavutamisel on inaktiivse angiotensiin I muundamine aktiivseks angiotensiiniks II angiotensiini konverteeriva ensüümi (ACE) abil ja angiotensiin II koostoime selle füsioloogiliste retseptoritega, sealhulgas AT1 retseptoritega. Angiotensiin II interakteerub vererõhu tõstmiseks AT1 retseptoritega. Selle süsteemi biokeemia ja füsioloogia tundmine pakkus teadlastele välja, et ebanormaalselt kõrge vererõhu alandamiseks võiks välja töötada uued ravimid.
ACE-d pärssinud ravim vähendaks angiotensiin II moodustumist. Angiotensiin II moodustumise vähenemine põhjustaks omakorda AT1 retseptorite aktiveerimise vähenemist. Seega eeldati, et AKE-d pärssivad ravimid alandavad vererõhku. See eeldus osutus õigeks ja töötati välja antihüpertensiivsete ravimite klass, mida nimetatakse AKE inhibiitoriteks. Samamoodi arvati, et kui AT1 retseptorite roll vererõhu säilitamises on aru saadud, avaldavad AT1 retseptoreid blokeerivad ravimid antihüpertensiivset toimet. Jällegi osutus see eeldus õigeks ja töötati välja antihüpertensiivsete ravimite teine klass, AT1 retseptori antagonistid. Agonistid on ravimid või looduslikult esinevad ained, mis aktiveerivad füsioloogilisi retseptoreid, samas kui antagonistid on ravimid, mis blokeerivad neid retseptoreid. Angiotensiin II on sel juhul AT1 retseptorite agonist ja antihüpertensiivsed AT1 ravimid on antagonistid. Hüpertensioonivastased ravimid illustreerivad uute ravimite sihtmärkide avastamise väärtust, mis on kasulikud suuremahulistes sõeluuringutes, et tuvastada plii kemikaale ravimite väljatöötamiseks.
Narkootikumide sõeluuring
Ühendite allikad
Keemiliste ühendite skriinimine võimalike farmakoloogiliste mõjude osas on väga oluline ravimite avastamise ja väljatöötamise protsess. Praktiliselt igal keemia- ja ravimiettevõttel maailmas on paljude aastakümnete jooksul sünteesitud keemiliste ühendite raamatukogu. Ajalooliselt on paljud erinevad kemikaalid saadud looduslikest toodetest, näiteks taimedest, loomadest ja mikroorganismidest. Ülikooli keemikutelt on saadaval veel palju keemilisi ühendeid. Lisaks on automatiseeritud, suure võimsusega, kombinatoorse keemia meetodid lisanud sadu tuhandeid uusi ühendeid. Kas mõnel neist miljonitest ühenditest on omadusi, mis võimaldavad neil saada narkootikumideks, tuleb veel kiire ja suure tõhususega ravimite sõeluuringute abil teada saada.
Plii keemiline identifitseerimine
Paul6 Ehrlichi aastaid kulus 606 kemikaali sõelumiseks, mille tulemuseks oli arsfenamiini väljatöötamine esimese tõhusa ravimina süüfilise raviks. Umbes Ehrlichi õnnestumise ajast (1910) kuni 20. sajandi teise pooleni tugines enamik potentsiaalsete uute ravimite sõelteste peaaegu eranditult tervete loomade, näiteks rottide ja hiirte ekraanidele. Ehrlich sõelus oma ühendeid süüfilisega hiirtel ja tema protseduurid osutusid palju efektiivsemaks kui tema kaasaegsed. Alates 20. sajandi teisest poolest on automatiseeritud in vitro sõelumismeetodid võimaldanud ühe päeva jooksul kümnete tuhandete keemiliste ühendite tõhususe skriinimist. Suure mahutavusega in vitro sõeltes segatakse üksikud kemikaalid ravimi sihtmärkidega mikrotiiterplaatide väikestes katseklaasitaolistes süvendites ja kemikaalide soovitav interaktsioon ravimi sihtmärkidega tuvastatakse mitmesuguste keemiliste meetoditega. Ekraanidel olevad ravimi sihtmärgid võivad olla rakuvabad (ensüümid, ravimite retseptorid, bioloogilised transporterid või ioonikanalid) või need võivad sisaldada kultiveeritud baktereid, pärmi või imetaja rakke. Kemikaalid, mis interakteeruvad soovitatavatel viisidel ravimite sihtmärkidega, saadakse müügivihjetena ja neid arendatakse edasi. Samuti võib sünteesida täiendavaid veidi muudetud struktuuriga kemikaale, kui pliiühend ei tundu olevat ideaalne. Kui juhtiv kemikaal on kindlaks tehtud, läbib see mitu aastat farmakoloogia ja toksikoloogia loomkatseid, et ennustada inimeste ohutust ja tõhusust tulevikus.
Looduslikest toodetest pärit pliiühendid
Teine väga oluline viis uute ravimite leidmiseks on kemikaalide eraldamine looduslikest toodetest. Digitalid, efedriin, atropiin, kiniin, kolhitsiin ja kokaiin puhastati taimedest. Kilpnäärmehormoon, kortisool ja insuliin eraldati algselt loomadest, penitsilliin ja muud antibiootikumid aga mikroobidest. Paljudel juhtudel kasutasid kogu maailmas asuvad põlisrahvad sadu või tuhandeid aastaid taimseid saadusi enne, kui tööstusriikide teadlased need „avastasid“. Enamikul juhtudel said need põlisrahvad teada, millised taimed on meditsiinilise väärtusega, samamoodi, nagu nad said teada, milliseid taimi oli ohutu süüa - katse ja eksitus. Etnofarmakoloogia on arstiteaduse haru, kus isoleeritud või primitiivsete inimeste kasutatavaid ravimeid uuritakse tänapäevaseid teaduslikke tehnikaid kasutades. Mõnel juhul isoleeritakse soovitavate farmakoloogiliste omadustega kemikaalid ja need muutuvad lõpuks ravimiteks, mille omadused on looduslikus tootes äratuntavad. Muudel juhtudel identifitseeritakse looduslikud tooted ainulaadsete või ebaharilike keemiliste struktuuridega kemikaalidega. Need uued keemilised struktuurid viiakse seejärel läbi ravimite skriinimisega, et teha kindlaks, kas neil on potentsiaalset farmakoloogilist või meditsiinilist väärtust. On palju juhtumeid, kus sellised keemilised struktuurid ja nende sünteetilised analoogid töötatakse välja ravimitena, mille kasutusotstarve erineb loodusliku toote kasutamisest. Üks selline ühend on oluline vähivastane ravimtaksool, mis eraldati Vaikse ookeani jugapuust (Taxus brevifolia).








![Richardsoni film "Maitse mett" [1961] Richardsoni film "Maitse mett" [1961]](https://images.thetopknowledge.com/img/entertainment-pop-culture/4/taste-honey-film-richardson-1961.jpg)