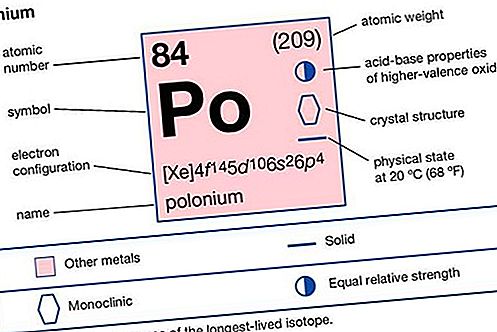
Hapniku rühma radioaktiivne, hõbehalli või musta metallelemendi polüoon (Po) (rühm 16 [VIa] perioodilises tabelis). Esimene element, mis radiokeemilise analüüsi abil avastati, polooniumi avastasid 1898. aastal Pierre ja Marie Curie, kes uurisid teatud pigi, uraanimaagi radioaktiivsust. Uraanile omistatavale väga intensiivsele radioaktiivsusele omistati uus element, mille nad nimetasid Marie Curie kodumaa Poola järgi. Avastusest teatati juulis 1898. Poloonium on äärmiselt haruldane, isegi pigilahus: 40 milligrammi polooniumi saamiseks tuleb töödelda 1000 tonni maagi. Selle arvukus maakoores on umbes üks osa 10 15-st. Looduses esineb see uraani, tooriumi ja aktiiniumi radioaktiivse lagunemissaadusena. Selle isotoopide poolestusajad ulatuvad sekundi murdosa kuni 103 aastani; kõige levinum loodusliku polüooniumisotoobi, poloonium-210, poolestusaeg on 138,4 päeva.
Poloonium eraldatakse tavaliselt uraani mineraalidest raadiumi ekstraheerimise kõrvalsaadustest. Keemiatööstuses isoleerimist Uraanipigimaak maagi töödeldakse vesinikkloriidhappega, ning saadud lahust kuumutatakse vesiniksulfiidi kuni sademe poloonium monosulfiidiks, positiivne, koos teiste metallisulfiidid, nagu seda on vismutit, Bi 2 S 3, mis meenutab poloonium monosulfiidiks keemilises käitumises tihedalt, kuigi see on vähem lahustuv. Lahustuvuse erinevuse tõttu kontsentreerib sulfiidide segu korduv osaline sadestumine polooniumit lahustuvamasse fraktsiooni, vismut aga koguneb vähem lahustuvatesse osadesse. Lahustuvuse erinevus on siiski väike ja täieliku eraldamise saavutamiseks tuleb protsessi korrata mitu korda. Puhastamine toimub elektrolüütilise sadestamise teel. Seda saab toota kunstlikult vismuti või plii pommimisega neutronite või kiirendatud laetud osakestega.
Keemiliselt sarnaneb poloonium telluuri ja vismuti elementidega. Polooniumist on teada kaks modifikatsiooni, α- ja β-vorm, mis mõlemad on toatemperatuuril stabiilsed ja omavad metallilisi omadusi. Fakt, et selle elektrijuhtivus väheneb temperatuuri tõustes, asetab polooniumit pigem metallide kui metalloidide või mittemetallide hulka.
Kuna poloonium on väga radioaktiivne - see laguneb plii stabiilseks isotoobiks, eraldades alfakiiri, mis on positiivselt laetud osakeste voog -, tuleb seda käsitseda eriti ettevaatlikult. Kui poloonium sisaldub sellistes ainetes nagu kuldfoolium, mis takistab alfakiirguse pääsemist, kasutatakse seda tööstuslikult staatilise elektri kõrvaldamiseks, mis on tekkinud sellistest protsessidest nagu paberi valtsimine, lehtplasti tootmine ja sünteetiliste kiudude ketramine. Seda kasutatakse ka fotofilmide tolmu eemaldamiseks harjadel ja tuumafüüsikas alfakiirguse allikana. Neutronite allikana kasutatakse polooniumisegusid berülliumi või muude kergete elementidega.
Elemendi omadused
| aatomnumber | 84 |
|---|---|
| aatommass | 210 |
| sulamispunkt | 254 ° C (489 ° F) |
| keemispunkt | 962 ° C (1764 ° F) |
| tihedus | 9,4 g / cm 3 |
| oksüdatsiooniseisundid | −2, +2, +3 (?), +4, +6 |
| elektronkonfiguratsioon. | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 2 6p 4 |