Süsiniku nukleofiilide lisamine
Aldehüüdidele lisab mitmesuguseid süsiniku nukleofiile ja sellised reaktsioonid on sünteetilises orgaanilises keemias esmatähtsad, kuna toode on kahe süsiniku skeleti kombinatsioon. Orgaanilised keemikud on nende reaktsioonide leidliku kasutamise abil suutnud kokku panna peaaegu ükskõik millise süsiniku skeleti, ükskõik kui keeruline. Üks vanimaid ja olulisemaid on Grignardi reagentide (RMgX, kus X on halogeeniaatom) lisamine. Prantsuse keemik Victor Grignard võitis nende reagentide ja nende reaktsioonide avastamise eest 1912. aasta Nobeli keemiapreemia.
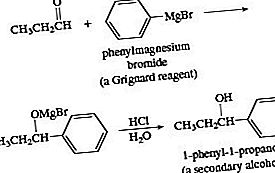
Grignardi reaktiivi lisamine aldehüüdile, millele järgneb hapestamine happe vesilahuses, annab alkoholi. Lisamine formaldehüüdile annab primaarse alkoholi. Lisamine lisaks aldehüüdile kui formaldehüüd annab sekundaarse alkoholi.
Teine süsiniku nukleofiil on tsüaniidi ioon, CN -, mis reageerib aldehüüdidega, saades pärast hapestamist tsüanohüdriine, ühendeid, mis sisaldavad OH ja CN rühma samal süsiniku aatomil.
Bensaldehüüdtsüanohüdriin (mandelonitriil) on huvitav näide keemilisest kaitsemehhanismist bioloogilises maailmas. Seda ainet sünteesivad millipeedid (Apheloria corrugata) ja säilitatakse spetsiaalsetes näärmetes. Millipeedi ähvardamise korral sekreteeritakse tsüanohüdriin selle säilitusnäärmest ja toimub ensüümide poolt katalüüsitud dissotsiatsioon vesiniktsüaniidi (HCN) saamiseks. Seejärel eraldab millipede HCN-gaasi ümbritsevasse keskkonda, et kiskjaid eemale hoida. Üksiku millipeedi eraldatud HCN kogus on piisav väikese hiire tapmiseks. Mandelonitriili leidub ka mõrudes mandlites ja virsikuhunnikutes. Selle funktsioon seal pole teada.
Muud olulised reaktsioonid selles kategoorias hõlmavad Knoevenageli reaktsiooni, milles süsiniku nukleofiil on vähemalt ühe a-vesinikuga ester. Tugeva aluse juuresolekul kaotab ester a-vesiniku, saades negatiivselt laetud süsiniku, mis lisab seejärel aldehüüdi karbonüülsüsinikule. Hapestamine, millele järgneb veemolekuli kaotamine, annab α, β-küllastumata estri.
Veel üks süsiniku nukleofiili sisaldav liitumisreaktsioon on Wittigi reaktsioon, milles aldehüüd reageerib fosforaaniga (mida nimetatakse ka fosforüliidiks), et saada ühend, mis sisaldab süsiniku-süsiniku kaksiksidet. Wittigi reaktsiooni tulemuseks on aldehüüdi karbonüülhapniku asendamine fosforiga seotud süsiniku rühmaga. Saksa keemik Georg Wittig jagas 1979. aastal Nobeli keemiapreemiat selle reaktsiooni avastamise ja selle kasutamise arendamise eest sünteetilises orgaanilises keemias.
Ühendid, mis sisaldavad Trimetüülsilüülrühma (-SiMe 3, kus Me on metüülrühm, -CH 3) ja liitium (Li) aatom sama süsiniku aatomiga reageerida aldehüüdidega nn Peterson reaktsiooni saades samu tooteid, mis oleks saadakse vastava Wittigi reaktsiooni abil.
Nihe α-süsiniku juures
α-halogeenimine
Α-vesinik aldehüüdi võib asendada kloori (Cl), broom (Br) või jood (I) aatom kui ühendit töödeldi Cl 2, Br 2 või I 2 vastavalt kas ilma katalüsaatorit või happelise katalüsaatori juuresolekul.
Pärast ainult ühe halogeeni aatomi lisamist saab reaktsiooni hõlpsalt peatada. α-halogeenimine toimub tegelikult aldehüüdi enoolvormil (vt ülalpool Aldehüüdide omadused: Tautomerism), mitte aga aldehüüdil endal. Sama reaktsioon toimub, kui lisatakse alus, kuid siis ei saa seda peatada enne, kui kõik sama süsiniku külge kinnitatud a-halogeenid on asendatud halogeeniaatomitega. Kui on olemas kolm α-vesinikku sama süsiniku reaktsioon on ühe sammu, mille tulemusel lõhustamisel X 3 C - iooni (kus X on halogeen) ja moodustamise soola karboksüülhape.

Seda reaktsiooni nimetatakse haloform reaktsiooni tõttu X 3 C - ioonid reageerivad veega või teise happe kinnipidamiseks süsteem toota ühendeid kujul X 3 CH, mida kutsutakse haloforms (nt CHCl 3 nimetatakse kloroform).